[fb_button]
Pomiar zasolenia
Jak, czym i dlaczego?
„Heureka” – „Znalazłem”, krzyknął Archimedes, odkrywszy znane dzisiaj wszystkim prawo. Często nie zdajemy sobie nawet sprawy, że właśnie wykorzystaliśmy odkrycie Archimedesa, ale kiedy dokonujemy pomiaru gęstości wody w akwarium, powinniśmy o nim pamiętać. Dla przypomnienia, definicja szkolna:
Na ciało zanurzone w cieczy działają dwie siły – siła ciężkości i siła wyporu, która skierowana jest przeciwnie do siły ciężkości i równa (co do wartości) ciężarowi cieczy wypartej przez to ciało.
Choć to prawo dotyczy też gazów, to dla potrzeb naszego hobby, skupmy się na cieczach.
Ujmując to we wzory w odniesieniu do pomiaru areometrem („spławikiem”)
Sc – siła ciężkości
Sw – siła wyporu
Ro1 – gęstość cieczy
Ro2 – gęstość ciała (areometru)
V1 – objętość cieczy, m1 – masa cieczy
V2 – objętość ciała, m2 – masa ciała (areometru)
g – przyspieszenie ziemskie
Sc = m2*g Sc = Ro2*V2*g
Sw = m1*g Sw = Ro1*V1*g
Sc=Sw
Ro2*V2*g = Ro1*V1*g Ro2*V2 = Ro1*V1
Ro1 = Ro2*V2/V1
Zakładając, że Ro2 i V2 dotyczą zamkniętego naczynia, jakim jest spławik, to jest to jakaś stała, charakterystyczna dla tego urządzenia, przyjmijmy „k”. Nie jest to do końca prawdą, bo szkło też podlega prawu rozszerzalności cieplnej, ale z uwagi na objętość, można to pominąć.
Czyli: Ro1=k/V1
Z powyższego wynika, że gęstość (Ro1) jest większa, jeśli objętość wypartej cieczy (V1) jest mniejsza (mniejsze zanurzenie spławika).
Należy jednak pamiętać, że od +4stC w górę (i w dół oczywiście) woda zwiększa swoją objętość i zmniejsza gęstość, dlatego:
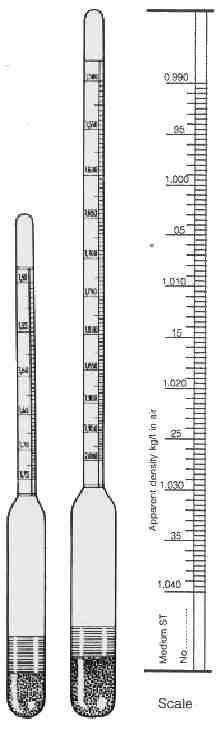
W ciepłej „rzadkiej” wodzie, spławik musi wyprzeć więcej wody, w związku z czym zatopi się głębiej, dając zaniżony odczyt.
To skąd się bierze ta „dodatkowa objętość” wypartej wody, przecież bańka salimetru jest cała zatopiona w wodzie? No właśnie ze skali, a właściwie rurki w której jest skala. To jest dodatkowa objętość dla siły wyporu, czyli ciężaru/objętości cieczy wypartej.
Co więc wpływa na dokładność spławika, bańka czy rurka ze skalą? Można powiedzieć, że jedno i drugie. W praktyce przelicza się stosunek objętości bańki do przekroju rurki (trzpienia). Im stosunek większy, tym areometr dokładniejszy. Dla areometrów o niskiej czułości przyjmuje się stosunek kilka do kilkudziesięciu, natomiast bardzo czułe areometry mają ten stosunek ok. 500-1000.
Tak więc, im większa bańka, tym więcej cieczy zostanie wyparte po jej zanurzeniu i mniej zostanie do wyparcia przez trzpień, co umożliwi wykonanie cienkiego trzpienia z długą, dokładną skalą. Innymi słowy – im cieńszy trzpień, tym mniej wypartej wody na długość zanurzenia trzpienia i możliwość „rozwleczenia” skali na większej długości.
Nie bez znaczenia jest też waga samego spławika. Im więcej ołowiu w spławiku, tym niżej umiejscowiony środek ciężkości. Dzięki temu salimetr łatwiej „postawić” w wodzie, urządzenie mniej kiwa się na boki, umożliwiając dokładny odczyt.
No dobrze, a co z areometrem uchylnym?
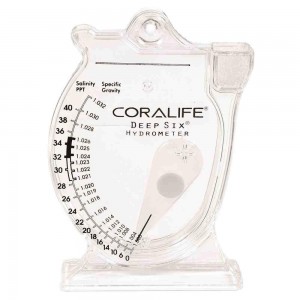
Prawie to samo, ale nie do końca. Zasada ta sama, prawo Archimedesa, tyle że objętość cieczy wypartej się nie zmienia, bo cała wskazówka jest już w wodzie. Objętość wypartej cieczy = objętość wskazówki. Co się zatem zmienia?
Zmienia się ciężar wypartej cieczy (konkretnej objętości), a z definicji jest on równy sile wyporu. Im gęstsza ciesz, tym większa siła wyporu i wskazówka porusza się ku górze, aż siła ciężkości zrównoważy siły działające w dół, czyli grawitację.
No dobrze, ale zgodnie z warunkami pływania ciał, ciało tonie, jeśli siła wyporu jest mniejsza od grawitacji, pływa po wierzchu, jeśli jest odwrotnie, lub pływa na dowolnej głębokości, jeśli siły się równoważą. To skąd w takim razie bierze się równowaga tych sił i konkretnie wskazana wartość?
Dzięki umocowaniu wskazówki do obudowy powstaje punkt obrotu i ramię, do którego przykładane są obie siły. Pomiar bez umocowania ograniczałby się więc do 3 stanów (gęstość wody większa, mniejsza, lub równa średniej gęstości wskazówki). Można w skrócie powiedzieć, że przyczepienie wskazówki do obudowy daje coś w rodzaju wagi z jednym ramieniem. Siła ciężkości (działająca w dół) jest stała, a siła wyporu (działająca w górę) zmienia się wraz z gęstością cieczy. Wskazanie jest więc wypadkową dwóch sił (sumą ich wektorów). Logiczne?
Ciekawym jest fakt, że tego typu hydrometry (nie wszystkie), nie wymagają korekcji temperatury i dają dość dokładne odczyty w warunkach akwarystycznych. (http://www.reefkeeping.com/issues/2004-07/rhf/)
No to dajmy na chwilę odpocząć Archimedesowi. Porozmawiajmy o świetle.
Powyższy schemat wyjaśnia wszystko. Każdy akwarysta wie, że łapiąc ryby w siatkę, trzeba wziąć pod uwagę kąt załamania światła przy przejściu z powietrza do wody. Ryba jest w zupełnie innym miejscu niż nam się wydaje, no chyba że patrzymy na nią prostopadle z góry. To zjawisko nazywane jest refrakcją, a odpowiednio zastosowane pozwala na pomiar gęstości wody.
Jak widać, załamanie światła następuje na granicy próbki i pryzmatu, i jest tym większe, im większa jest różnica gęstości ośrodków (szkła i wody), a właściwie ich współczynników załamywania światła (indeksów refrakcji).
Strzałka w lewym dolnym rogu symbolizuje promień świetlny, powiedzmy graniczny, który ulegnie załamaniu. Jeśli indeksy refrakcji będą bardzo różne, to ostatni promień jaki zobaczymy będzie ten oznaczony (a). Jeśli współczynniki refrakcji będą zbliżone, to ostatnim załamanym promieniem będzie promień (b).
Należy tylko pamiętać, że obserwujemy wiązkę światła, nie pojedynczy promień, dlatego oświetleniu ulega cały biały obszar, a nie punkt lub linia. Schematycznie i „całościowo” wygląda to następująco:
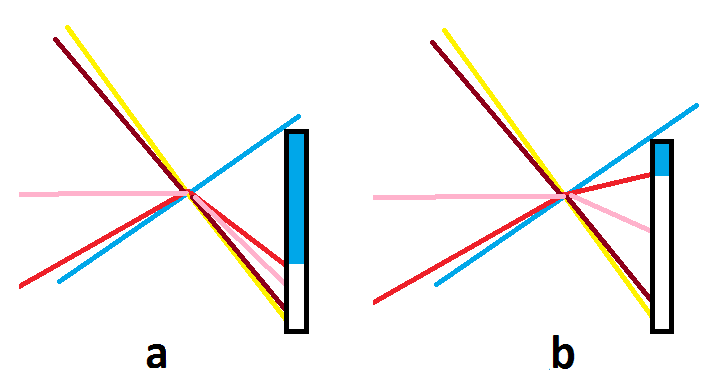
Niebieska linia – powierzchnia pryzmatu, na której jest próbka, żółta linia – promień prostopadły do powierzchni styku (nie ulega załamaniu), linie brązowa, różowa i czerwona – strumień światła (promienie wpadają pod różnym kątem i ulegają różnemu załamaniu). Cały czas pamiętamy, że chodzi o różnice współczynników refrakcji szkła i wody, więc jeśli te współczynniki będą równe, to „czerwony promień wyprostuje się” (cała reszta też) i oświetleniu ulegnie cała skala.
Proste, prawda? No, ale znowu pojawia się problem temperatury i gęstości – większa temperatura to mniejsza gęstość (i współczynnik refrakcji) i odwrotnie.
Na styku rzadkiej „ciepłej” wody i pryzmatu dojedzie do większego załamania promieni świetlnych, co da zaniżony odczyt.
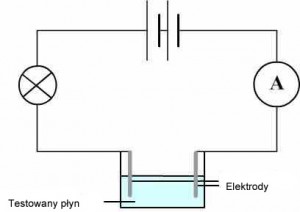
A może można inaczej? – Można… Prąd, elektrolit…
Pomiar zasolenia możliwy jest też przez określenie przewodności elektrycznej (Conductivity). Wykorzystany jest tutaj fakt, że elektrolity, czyli substancje w których oprócz rozpuszczalnika występują jony, mają zdolność do przewodzenia prądu. Im więcej jonów, tym lepsze przewodzenie, woda bardzo czysta prawie nie przewodzi prądu.
Conductance i Conductivity to co innego. Conductance wyrażana jest w jednostkach Simens (S), czyli Amper/Volt (jako odwrotność oporu – ohm, często zapisywana – mho), Conductivity dodatkowo przeliczona jest na odległość miedzy elektrodami, czyli np. mS/cm. Mając źródło o znanym napięciu (U), wykonujemy pomiar prądu (I) przepływającego pomiędzy elektrodami umieszczonymi w pewnej odległości od siebie, a dzięki specjalnym tabelom określamy zasolenie:
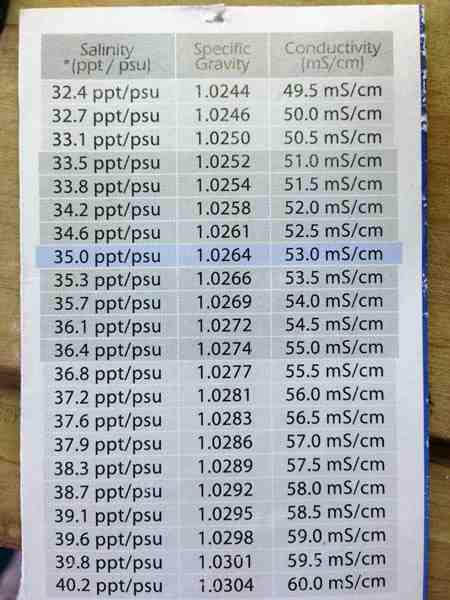
I tu uwaga:
Wraz ze wzrostem temperatury, rośnie przewodniość (bo jony szybciej się poruszają), co da zawyżony odczyt. Odwrotnie niż w poprzednich metodach ;-)
Co zatem zrobić, aby odczytywać dokładnie co mamy w akwarium? Może lepiej w pierwszej kolejności ustalić, o czym chcemy mówić, jaką informację chcemy przekazać.
Zaczynając od początku, Archimedes powiedziałby pewnie „zanurzając ciało, wylałem 2 litry wody z wanny” (zakładam, że nie jest to ciało Archimedesa, aby łatwiej przedstawić zależności ;-) ). Miałby rację, ale to nic nie mówi o zasoleniu tej wody. Niezależnie, jaka to będzie woda, będzie to tyle samo wody, no chyba że z racji dużej gęstości wody całkowite zanurzenie tego ciała będzie niemożliwe. Jednak Archimedes wyciągnął jeszcze jeden wniosek – ciężar cieczy wypartej jest równy sile wyporu. Mógłby też więc powiedzieć w tym przypadku „wyparłem 2,046kg wody” i to już jest jakaś informacja. Jeśli połączymy obydwie informacje, jesteśmy w stanie określić gęstość tejże wody:
Ro1 = m/V = 2,046kg/2l = 1,023kg/l = 1,023g/cm3
– czyż nie o to chodziło? Mamy gęstość bezwzględną (Density), heureka. Ale wcześniej mówiliśmy, że może nam tu namieszać temperatura. 2,046kg wody będzie miało inną objętość w temperaturze 4stC, a inną w 26stC i odwrotnie – ta sama wyparta objętość będzie miała różną masę w różnych temperaturach. Dlatego określając gęstość wody, powinniśmy dodać „w temperaturze…” – 1,023kg/l w temperaturze 25stC – i już morszczak się cieszy, jeśli wie, że jest to gęstość odpowiednia. Warunkiem uśmiechu będzie jednak pomiar objętości i masy wykonany dokładnie w 25stC.
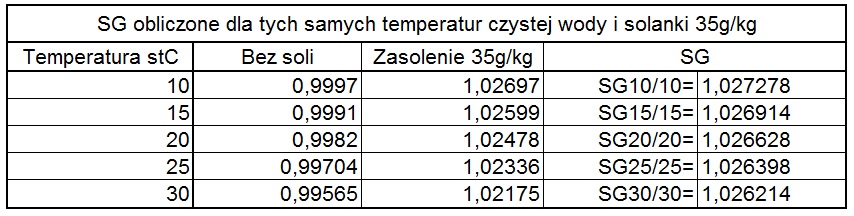
Z różnych przyczyn, a głównie do określenia pływalności, przyjęło się używać gęstości względniej (SG, Specific Gravity, Relative Density). Jest to nic więcej, jak stosunek gęstości bezwzględnej cieczy do gęstości bezwzględnej czystej wody, zwykle oba pomiary wykonywane są w tej samej temperaturze. Używając SG porównujemy gęstości dwóch cieczy. Odnosząc to do pływalności, ciało o SG>1 tonie, SG SG=(Roz/RowY)x1000
Roz – gęstość zmierzona (przyjmijmy wcześniejszy przykład 1,023g/cm3 w 25stC)
RowY– gęstość wzorca (czysta woda w temperaturze Y)
Row15,56 = 0,9990166g/cm3 SG = 1,0243
Row20,0 = 0,998203g/cm3 SG = 1,02519
Row25,0 = 0,997047950g/cm3 SG = 1,02637
Może też być Row3,98, gdzie gęstość = 1 i wtedy SG = Roz
Należy zwrócić uwagę, że podczas dzielenia znikają jednostki i dlatego, jeśli spotykamy wartość 1,025 (20stC) to wiemy że chodzi o SG, jeśli pojawią się jednostki (g/cm3 w 20stC), to mowa o gęstości.
Żeby nie było tak łatwo, to należy zwrócić uwagę, że przy SG w zasadzie odnosimy się do dwóch temperatur : pierwsza – temperatura pomiaru, która wpływa na gęstość zmierzoną i druga – temperatura odniesienia (temperatura czystej wody), określona w czasie kalibracji. Dla powyższych obliczeń, aby nie było wątpliwości, zapisy powinny wyglądać następująco:
1,023 (25/4stC); 1,0243 (25/15,56stC); 1,02519 (25/20stC); 1,02637(25/25stC)
Jak widać, mówimy cały czas o tej samej próbce wody i pomiarach wykonanych w tych samych warunkach, a SG (gęstość względna) waha się od 1,023 do 1,026, zależnie od użytego sprzętu.
Użyłem przed chwilą słowa „kalibracja”, które w świetle powyższego nie tyle traci sens, co nabiera dodatkowego znaczenia. Kalibracja odnosi się bowiem do korekcji ustawień sprzętu, a nie do przeliczeń, które przed chwilą wykonaliśmy. „Y” w zapisie X/YstC, mówi nam o temperaturze czystej wody względem której porównujemy naszą próbkę o temperaturze X. Jeśli więc jesteśmy szczęśliwymi posiadaczami spławika, który ma napisane 25stC (77stF) i w akwarium mamy taką samą temperaturę, to możemy śmiało powiedzieć, że prawidłowo odczytujemy SG.
http://www.theaquariumsolution.com/measuring-salinity-and-specific-gravity-your-aquarium
Wniosek, jaki należy z tego wyciągnąć, jest następujący: Aby poznać prawdziwe parametry wody, trzeba wiedzieć co dany pomiar nam mówi, a następnie dokonać odpowiednich obliczeń. Nie ma znaczenia, czy posługujemy się gęstością (density), czy gęstością względną (relative density, czyli SG), ważne jest, abyśmy umieli te wartości skorygować i porównać.
Na pytanie, co w takim razie mój sprzęt mierzy, musi sobie odpowiedzieć sam użytkownik. Moim zdaniem (ale to tylko moje zdanie, bo głosy są podzielone), jeśli nie napisano na sprzęcie że jest to SG i nie określono temperatury, to musi to być gęstość. Poza tym, bez podania temperatury wzorca, podawanie gęstości względnej nie ma sensu. Dlaczego? A dlatego, że SG używane jest do określania pływalności. Żeby tę pływalność określić, powinniśmy porównać gęstości obu ciał w tej samej temperaturze, czyli np. 20/20stC (co często zapisuje się jednym 20stC). Można to odnieść do sytuacji ze statkiem, który płynąc z zimnych wód do ciepłych nagle zaczyna tonąć, bo ktoś źle określił wyporność (głębokość zanurzenia – ilość wypartej wody, w zależności od zmian gęstości wody).
Wracając do jednostek. Każdy co jakiś czas staje przed koniecznością wykonania podmiany wody. Na początku mojej przygody z akwarystyką, kiedy kupiłem pierwszy „spławik”, dość często przy okazji podmian, korygowałem gęstość wody w akwarium. Teraz wiem, że prawdopodobnie, w większości przypadków, korygowałem zupełnie niepotrzebnie, a „złe wyniki” otrzymywałem z powodu różnych temperatur pomiaru. Im bardziej korygowałem, tym gorsze były efekty, zarówno mierzalne jak i wizualne ;-). Błędów popełniałem wiele, a wszystkie nakładały się na siebie, powiększając „błąd ostateczny”. Pierwszy błąd – pomiar w zbiorniku, drugi błąd – korekcja tego pomiaru, trzeci błąd – pomiar w zrobionej solance, czwarty – korekcja tego pomiaru, kolejne dwa błędy to przeliczenie gęstości na ilość gramów soli, co było największym problemem.
Konia z rzędem temu, kto powie bez tabel i przeliczeń, ile wsypać soli do 100l wody, żeby podnieść SG z 1,024 do 1,026 (26/25stC)? Trzeba wiedzieć, ile jest gramów soli w litrze i ile chcemy mieć ostatecznie, reszta to prosta matematyka. Niestety gęstość nic nam na ten temat nie mówi. Rozwiązaniem tego problemu jest określanie zasolenia w Skali Praktycznej (PSU – Practical Salinity Unit). Nie chcę nikogo przekonywać, że jest to jedyna słuszna skala, ale praktyczna ona jest nie tylko z nazwy.
Krótko o tym co to PSU, czyli jak zrobić solankę.
Zasolenie w skali praktycznej, to stosunek przewodnictwa elektrycznego danej próbki wody morskiej w temperaturze 15stC i przy ciśnieniu 101325Pa, do przewodnictwa elektrycznego wzorca, którym jest wodny roztwór chlorku potasu 32,456g/1000g roztworu, w tych samych warunkach.
Brzmi fajnie ;-), ale okazuje się, że nie jest to tak skomplikowane, bo 35 PSU= 3,5% = 35‰ = 35g/kg = 35ppt. To dla mnie jest rzeczywiście praktyczna informacja, bo jeśli chcę mieć zasolenie 35g/kg, a mam 34g/kg, to wiem, że do każdego kilograma roztworu NaCl muszę wsypać 1 gram soli, czyli do 100l wsypię 100g (jest to pewne uproszczenie, o którym za chwilę).
Powyższe, nie do końca jest prawdą, gdyż takie rozumowanie odnosi się do czystego NaCl, a sól morska czystym NaCl nie jest. To też nie jest problem. Mając przyrząd do pomiaru zasolenia, możemy łatwo określić „Salinity factor” danej soli. Rozpuszczamy np. 300g soli w 10l wody, czyli 30g/l mierzymy zasolenie i otrzymujemy np. 25g/l. Salinity factor = 25g/30g=0,833. Skoro wiem, że muszę dodać 100g NaCl do sytemu, to dzielę to przez Salinity factor i otrzymuję 100g/0,833=120g „morskiej soli”.
Dokładnie takie same obliczenia można wykonać podczas podmianki, tylko trzeba odjąć to co wyjmuje się z systemu zastępując „dobrą solanką” + uzupełnienie gramów na pozostałą część wody. Powiedzmy 10% ze 100l z powyższego przykładu – ubywa 10l, do którego przygotowania trzeba wziąć 350g/0,833=420g i do każdego z pozostałych 90l pozostałych trzeba dodać po 1g/0,833=1,2g, czyli 1,2g*90l=108g, co w sumie daje 420g+108g=528g „morskiej soli”.
Praktyczna uwaga, Salinity factor proponuję liczyć przy każdej podmiance, wsypując najpierw trochę mniejszą ilość soli, np. 300-350g/10l RO, policzyć Salinity factor, a następnieobliczyć ilość soli jaką powinniśmy wsypać do uzyskania docelowego zasolenia, pamiętając o tym, co już wsypaliśmy.
Pisałem wcześniej, że stosujemy pewne uproszczenie, tak więc pytanie: Czy g=ml? Oczywiście, w przypadku solanki – NIE, lecz w pewnych sytuacjach takie uproszczenie nie wpływa znacząco na wynik ostateczny. 1litr wody morskiej o temperaturze 25stC i o zasoleniu 34g/kg waży waży 1,0256kg, a o zasoleniu 35g/kg waży 1,0264kg, czyli zawierają odpowiednio 34,87g/l i 35,92g/l suchej soli. Różnica wynosi więc 1,05g/l, zamiast 100g/100l powinienem dosypać 105g/100l NaCl (126g soli morskiej uwzględniając Salinity factor). Jak widać, przy tak małej korekcji zasolenia, takie przybliżenie można zastosować, czyli g/kg = g/l. Jeśli jednak będziemy chcieli korygować zasolenie o większe wartości, należy wziąć powyższe pod uwagę.
Dość matematyki, wróćmy do pomiarów.
Wielokrotnie wspominałem już, że temperatura ma duże znaczenie przy naszych pomiarach. Jak więc uniknąć błędów?
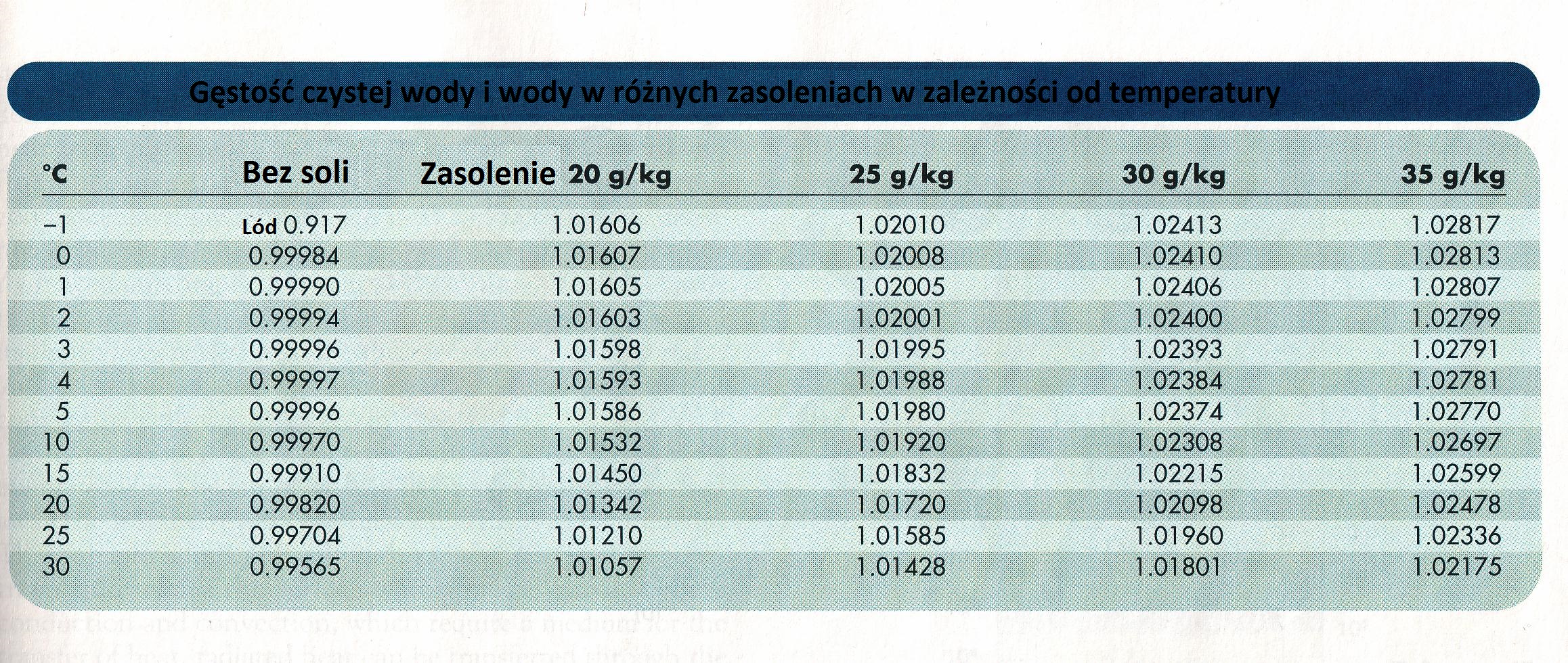
Zaopatrzyć się w dobry termometr, oraz w tabele/programy, dzięki którym obliczymy rzeczywiste parametry. Dla przykładu:
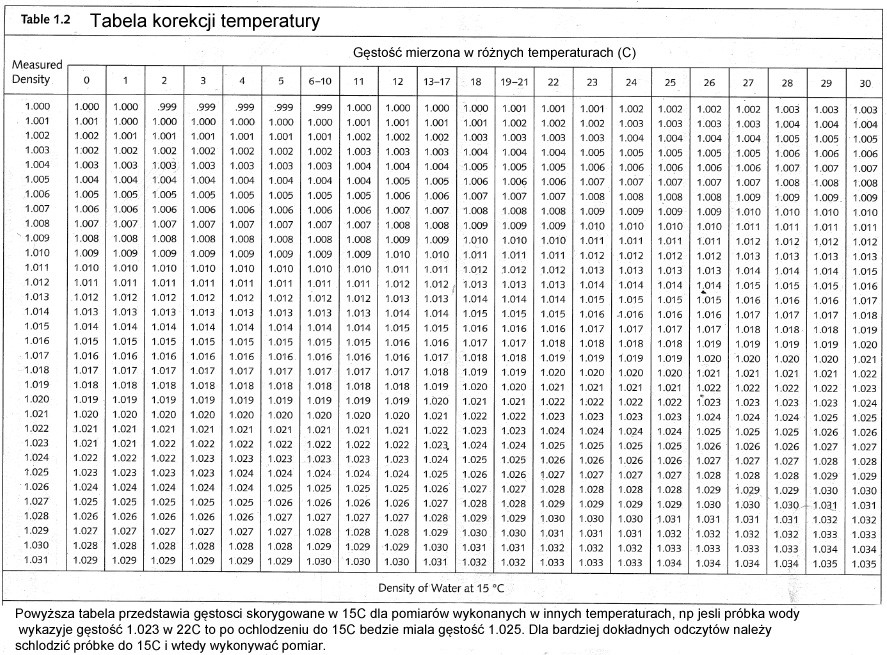
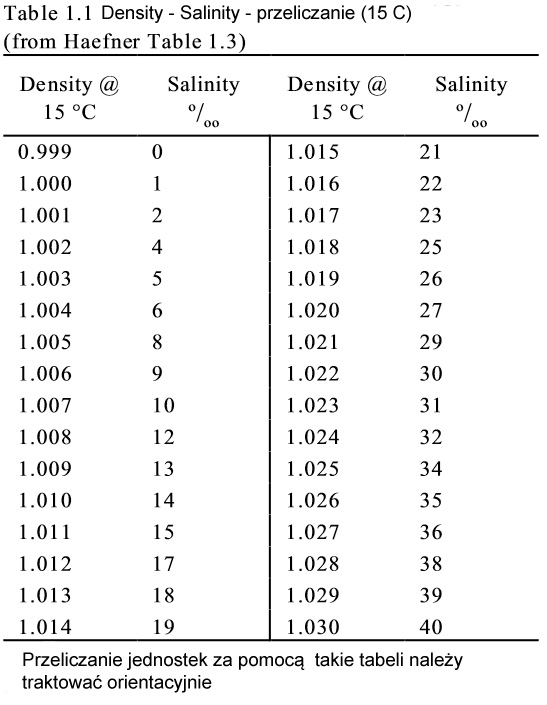
Jeśli wykonamy pomiar gęstości, np. 1,024g/cm3 w 25stC, otrzymany wynik znajdujemy w pierwszej kolumnie tabeli 1 (Measured Density) i szukamy temperatury pomiaru 25stC. Na skrzyżowaniu rzędu i kolumny widzimy wynik, czyli 1,026g/cm3 w temp. 15stC. Z tabeli 2 odczytujemy, że 1,026g/cm3 w temp. 25stC to 35‰
Tabela 1: Przeliczanie gęstości bezwzględniej zmierzonej w różnych temperaturach do gęstości w temperaturze 15stC.
Tabela 2: Przeliczanie gęstości bezwzględnej zmierzonej w 15stC na zasolenie wyrażone w ‰
Oczywiście obie tabele można złożyć w jedną, niestety takiej wersji nie znalazłem.
Jak zwykle, diabeł tkwi w szczegółach – czyli przybliżeniach, które wykonaliśmy 2x, a prawdopodobnie nawet 4x – 2 razy przeliczając, i 2 razy określając temperaturę i odczytując ze spławika.
A propos odczytywania ze spławika, to odczyt powinien być brany z poziomu tafli wody (dół menisku), nie „dokąd sięgnie woda”.
Co w takim razie z SG? Tak samo, trzeba tylko mieć tabele dla różnych kombinacji, jak różne są „spławiki”. Ponieważ zwykle pomiaru dokonujemy w temperaturze 25stC, to i spławik powinien podawać SG względem czystej wody w temperaturze 25stC(77stF), tak jak Tropic Marin High Precision Hydrometer (i powinno być to wyraźnie napisane). Jeśli będziemy musieli wykonać pomiar w innej temperaturze niż 25stC, do obliczenia zasolenia musimy wykonać korekcję używając poniższej tabeli:Źródło: http://www.reefkeeping.com/issues/2004-07/rhf/#c
O, i w tym miejscu należy zauważyć, że wszystkie nasze metody pomiaru sprowadzają się ostatecznie do jednego – określenia ilości soli w wodzie. Pomiar bezpośredni (odparowanie jakiejś objętości i zważenie suchej soli) jest dość trudne, dlatego żeby otrzymać to co nas interesuje musimy posłużyć się metodami pośrednimi i przejść przez kilka etapów przeliczeń i zaokrągleń.
Życie można sobie jednak ułatwić i zamiast zaglądać do tabel, wystarczy zakupić urządzenie z kompensacją temperatury i najlepiej pokazujące zasolenie w PSU. Tylko co to jest tak naprawdę ta kompensacja?
Kompensacja, to nie jest pomiar w tej temperaturze, to tylko „sprowadzenie” / przeliczenie do danej temperatury. Jak to się dzieje – sprawa bardzo prosta – przesuwa się skala. Co prawda, w przypadku popularnych spławików czy areometrów uchylnych przesunięcie skali jest stałe, więc i kompensacja kiepska, natomiast w przypadku refraktometrów z ATC sprawa wygląda następująco:
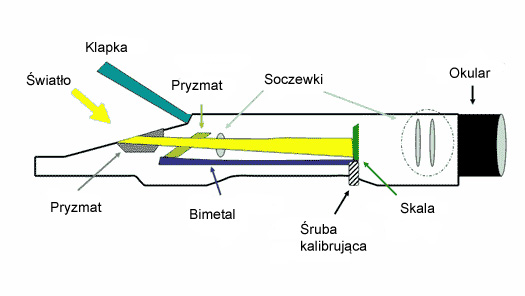
Kropla wody położona na pryzmat przyjmuje temperaturę refraktometru, czyli otoczenia. W zależności od temperatury otoczenia Bimetal „wygina się” przesuwając skalę w odpowiednim kierunku, tak aby mimo temperatury otoczenia 4, czy 30stC, podana wartość była zbliżona do pomiaru w temperaturze 20stC (o ile na refraktometrze napisano 20stC lub D20/20). W efekcie tego zabiegu otrzymujemy gęstość względną próbki w temperaturze 20stC, względem czystej wody w tej samej temperaturze. Obchodzi nas jednak gęstość w 25stC, dlatego niestety, ale w przypadku kiedy na refraktometrze napisane jest D20/20, to mimo kompensacji temperatury, celem określenia gęstości w 25stC (jakiejkolwiek, względnej czy bezwzględnej) powinniśmy posłużyć się tabelami. Większość nowoczesnych refraktometrów, dedykowanych do pomiaru SG dla wody morskiej (nie roztworów NaCl) podaje SG, które jest bardzo zbliżone do SG w temperaturze 25stC. Do zrobienia solanki mając tylko SG, znowu trzeba przeliczać.
Na szczęście większość refraktometrów posiada też skalę zasolenia w PSU (‰) i tu już sprawa jest prosta. Wartość zasolenia nie zależy bowiem od temperatury i nie ważne, w jakiej temperaturze wykonany jest pomiar, 35g/kg będzie zawsze 35g/kg. Zapyta ktoś pewnie teraz, po co w takim razie do takiego pomiaru kompensacja temperatury, skoro wynik od temperatury jest niezależny. Wynik rzeczywiście jest niezależny, ale sposób jego powstawania ma dużo wspólnego z temperaturą. Współczynnik refrakcji, czyli załamanie światła (Refractive Index) jest zależny od temperatury, dlatego mechanizm ATC przesuwa skalę tak, aby niezależnie od temperatury próbki, otoczenia, korygować załamanie światła, podając rzeczywisty wynik. Tak otrzymany wynik nie wymaga już żadnych dodatkowych zabiegów i w każdej temperaturze jest prawdziwy.
Dla mnie, świeżo upieczonego na tamten czas „morszczaka”, było to odkrycie na wagę wynalezienia koła. Nie chcę przekonywać nikogo, że jest to jedyna słuszna droga oceny zasolenia, ale w moim przypadku skończyły się problemy z zasoleniem i zrozumiałem ideę robienia solanki. Mam nadzieję, że dzięki temu opracowaniu część kolegów spojrzy inaczej na wykonywane pomiary i zrozumie odczytywane wyniki.
Pozostaje jeszcze jedno, kluczowe pytanie. Czy skład wody (poza NaCl) wpływa na ciężar właściwy / gęstość roztworu / pomiar zasolenia?
Oczywiście, że tak. Różne substancje mają różną gęstość, czyli stosunek wagi do objętości. Nie wdając się w szczegóły, w związku z powyższym, inną wagę będzie miał roztwór 1kg NaCl 10l wody i 1kg CaCl2 w 10l wody. Mam nadzieję, że zastanawialiście się, dlaczego robiąc odczynniki do Ballinga nie wlewamy np. 5 litrów wody, tylko dopełniamy do 5 litrów? Wlewając równą ilość wody, w każdym pojemniku byłaby inna objętość, ale to nie temat na teraz.
Pomiar gęstości nie odnosi się tylko do NaCl w wodzie morskiej, ale do wszystkiego co tam się znajduje. Jony Sodu, Magnezu, Chloru i Siarczany to ok. 97% masy jonów rozpuszczonych. Każde zachwianie równowagi odbije się na zasoleniu. Dla przykładu, roztwór bromku potasu o SG równym wodzie morskiej ma „zasolenie” około 36ppt, taki sam roztwór siarczanu magnezu ma “zasolenie” tylko 26ppt. (cyt.: http://www.reefkeeping.com/issues/2004-07/rhf/#c). Dlatego właśnie twierdzenie: „Zasolenie mam dobre, ale magnez za wysoki” jak i „Magnez ok., mimo złego zasolenia” dalece mijają się z prawdą i to bez względu na wybraną metodę pomiaru (grawitacyjną, czy za pomocą refrakcji). Temat został wyczerpująco opracowany tutaj:
http://reefkeeping.com/issues/2006-12/rhf/#6 – zachęcam do lektury.
To co w cytowanych pracach wielokrotnie jest powtarzane i co czuję się zobowiązany w tym opracowaniu wyraźnie podkreślić, to temat kalibracji.
Przede wszystkim kompensacja i kalibracja to dwie różne rzeczy. Wróćmy na chwilę do rysunku refraktometru. Śruba kalibracji ustawia skalę w odpowiednim miejscu, tak aby kompensowany przez bimetal pomiar był adekwatny do pomiaru w określonej temperaturze (temperaturze kompensacji, np. 20stC). Gdyby kompensacji nie było, pomiar musielibyśmy wykonywać w temperaturze 20stC, lub zaznaczyć, że próbka (otoczenie) miało inną temperaturę, oczywiście pomiar też byłby adekwatny do temperatury próbki. Jasnym staje się więc, że kalibracja urządzenia bez kompensacji musi być wykonana w warunkach, w których pomiar będzie wykonywany i najlepiej, jeśli przed każdym pomiarem wykonamy kalibrację. Dzięki kompensacji, kalibrację możemy wykonać w zasadzie w dowolnej temperaturze i raz na jakiś czas. Jednak kompensacja jest też „zabiegiem z pewnym przybliżeniem”, a przybliżenie jest tym dokładniejsze, im bardziej płyn kalibrujący zbliża się swoimi właściwościami do właściwości roztworu, który będziemy potem testować (skład, temperatura). O tym, że skład roztworu wpływa na wykonywane pomiary i kalibrację niech jeszcze świadczy fakt, że indeks refrakcji NSW (Natural Seawater) przy zasoleniu 35ppt = 1.3394, natomiast roztwór czystego NaCl z tym samym współczynnikiem refrakcji będzie miał zasolenie 36,5ppt. Stąd wniosek, że aby w miarę poprawnie skalibrować refraktometr, należy użyć roztworu NaCl zrobionego z 36,5g chlorku sodu i 963,5g wody z RO (ważne!!! Nie 1000ml wody, bo to nie to samo!!!)
Na zakończenie, jeśli zasiałem ziarenko niepewności u kogoś, komu się wydawało, że wie co robi, to się cieszę. Zachęcam do szukania, czytania, poddawania pod wątpliwość tego, co uważane jest za pewnik, wyciągania wniosków i dyskusji. Najgorsze, to założyć że wie się już wszystko. Przyznam się, że pomysł napisania tej pracy powstał w chwili, kiedy zacząłem drążyć temat gęstości wody, mimo że od dłuższego czasu posługiwałem się PSU. Wiele się nauczyłem, mimo to nadal mam niedosyt i wydaje mi się, że to nie wszystko, dlatego…
Nie zalecam korekcji, jeśli wszystko jest ok., ale jeśli coś komuś nie wychodzi, to może warto zweryfikować spojrzenie na pomiary zasolenia.
Piotr Staniewski